Interview mit Dr. Andreas Raab

Im ersten Teil unserer Serie haben Sie uns die „Hallmarks of Aging“ vorgestellt, die uns das wissenschaftliche Verständnis des Alterns erleichtern und uns Hinweise geben, wie wir den Alterungsprozess verlangsamen können.
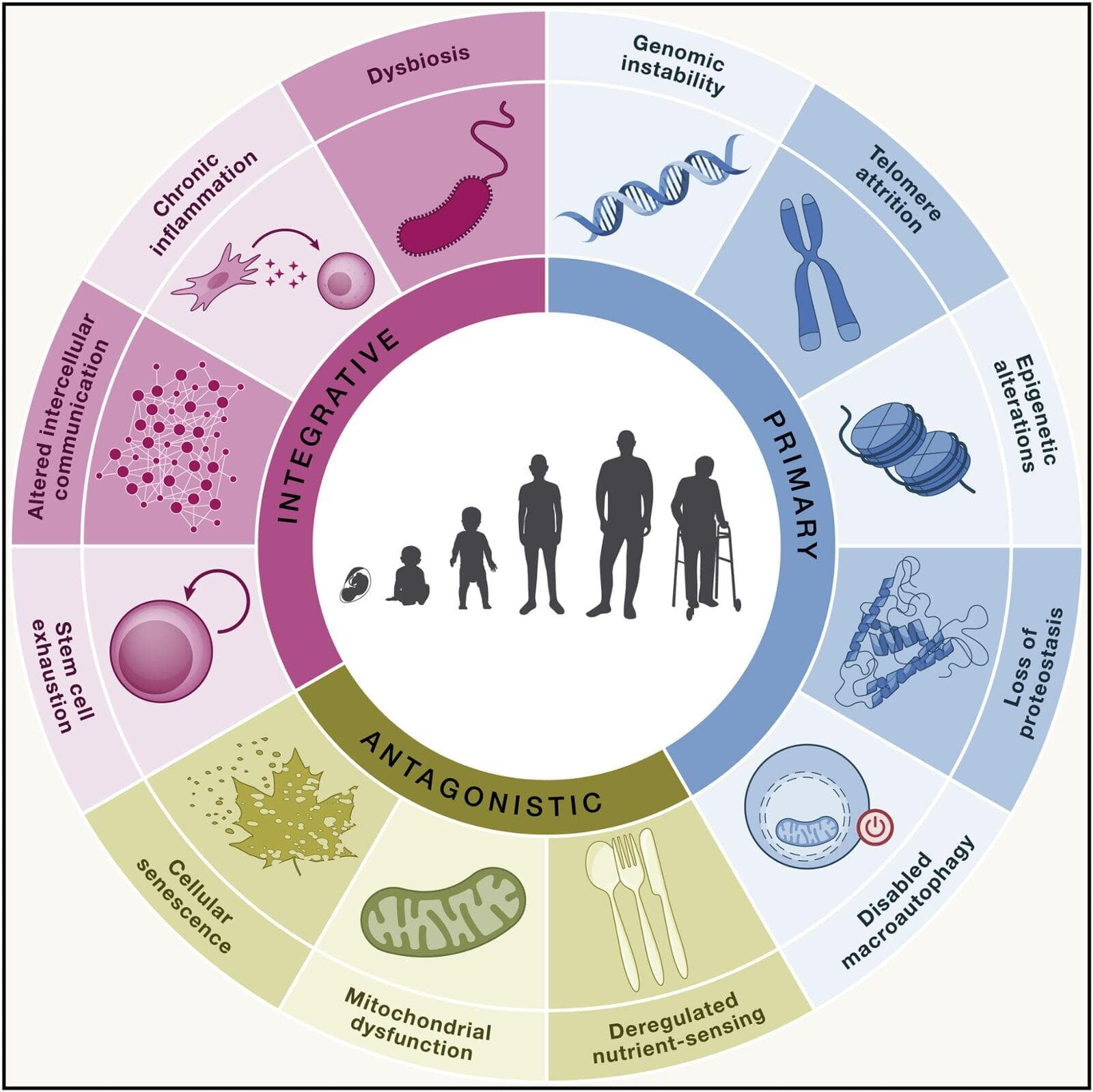
Heute möchten wir uns genauer mit den ersten zwei der zwölf „Hallmarks“ beschäftigen: der genetischen Instabilität und der Telomer-Abnutzung.
Genetische Instabilität
Bernhard Sillich (BS): Bitte erklären Sie uns zunächst, was der Begriff „genetische Instabilität“ bedeutet?
Dr. Andreas Raab (AR): Sehr gerne, Herr Sillich. Genetische Instabilität bezieht sich auf die Zunahme von Veränderungen und Schäden in unserem Erbgut, also der DNA, die im Laufe des Lebens auftreten. Solche Veränderungen können auf unterschiedliche Weise entstehen, zum Beispiel durch sogenannte Strangbrüche, bei denen die DNA-Fäden, die unsere Erbinformation tragen, an einer oder mehreren Stellen reißen. Ebenso können Basentauschfehler auftreten, bei denen einzelne Bausteine der DNA falsch zusammengefügt werden. In extremen Fällen gehen sogar ganze DNA-Segmente verloren.
Diese Schäden führen dazu, dass sich Mutationen anhäufen – also Veränderungen in der genetischen Information, die weitergegeben werden, wenn die Zelle sich teilt. Besonders problematisch ist es, wenn solche Mutationen in Keimzellen, also den Zellen, die an der Fortpflanzung beteiligt sind, oder in Stammzellen auftreten. Hier können sie sich dauerhaft im Organismus festsetzen und so die Grundlage für Krankheiten wie Krebs schaffen. Der Verlust von wichtigen Genabschnitten und die fehlerhafte Reparatur von DNA-Schäden beeinträchtigen die Funktion der Zellen. Dies führt dazu, dass Zellen ihre Aufgaben nur noch eingeschränkt erfüllen können und der Alterungsprozess beschleunigt wird.
Krebs entsteht beispielsweise, wenn Mutationen Gene betreffen, die das Zellwachstum und die Zellteilung regulieren. Wenn solche Gene geschädigt sind, verlieren die Zellen ihre normale Wachstumshemmung und beginnen, sich unkontrolliert zu vermehren. Daraus können sich Tumore entwickeln, die wiederum auf andere Organe übergreifen und lebensbedrohlich werden können.
Was wir dagegen tun können
BS: Das klingt sehr komplex und alarmierend. Können wir denn selbst etwas tun, um unsere DNA zu schützen und die genetische Instabilität zu verringern?
AR: Absolut! Auch wenn genetische Instabilität ein natürlicher Teil des Alterns ist, können wir durch bestimmte Verhaltensweisen und eine angepasste Lebensführung dazu beitragen, Schäden an unserer DNA zu vermeiden oder zumindest zu reduzieren.
Äußere Einflüsse
Ein wichtiger Faktor ist es, äußere Einflüsse zu minimieren, die unsere DNA schädigen. Dazu gehören beispielsweise UV-Strahlung, Röntgenstrahlung und die Verwendung von Kontrastmitteln bei bestimmten medizinischen Untersuchungen. Solche Einflüsse können das Risiko für DNA-Schäden und somit für Mutationen deutlich erhöhen.
Ein weiterer wichtiger Aspekt ist die Vermeidung von chemischen Stressoren wie dem Rauchen. Tabakrauch enthält viele schädliche Substanzen, die die DNA direkt angreifen und die genetische Instabilität fördern. Auch der Konsum von stark verarbeiteten Lebensmitteln und übermäßiger Alkoholkonsum sollten vermieden werden.
Faszinierenderweise verfügt unser Körper über umfassende DNA-Reparatur-Mechanismen, die Schäden erkennen und ausbessern können. Diese Reparaturprozesse funktionieren jedoch im Alter immer schlechter, was die Wahrscheinlichkeit von dauerhaften Schäden erhöht.
Lebensstiländerungen
Längere Nahrungspausen, wie beim intermittierenden Fasten, können eine unterstützende Rolle spielen: Untersuchungen haben gezeigt, dass durch Fasten bestimmte Proteine wie die Sirtuine aktiviert werden, die wiederum die DNA-Reparatur-Mechanismen anregen. Diese Proteine helfen dabei, DNA-Schäden effizienter zu beheben und tragen so dazu bei, die genetische Stabilität zu fördern.
Auch ein gesunder Lebensstil mit ausreichender Bewegung und der Vermeidung von unnötigen chemischen Belastungen kann dazu beitragen, die genetische Instabilität zu verringern. Besonders wertvoll sind Antioxidantien aus frischem Obst und Gemüse, da sie freie Radikale neutralisieren, die ansonsten die DNA angreifen könnten.
Telomer-Abnutzung
BS: Ein weiteres zentrales „Hallmark“ ist die Telomer-Abnutzung. Was genau versteht man darunter?
AR: Telomere sind spezialisierte Kappen auf den Enden unserer Chromosomen. Man kann sie sich wie die Schutzkappen an den Enden von Schnürsenkeln vorstellen, die verhindern, dass diese ausfransen. Bevor eine Zelle sich teilt, muss der gesamte Chromosomensatz, der aus 46 Chromosomen besteht (außer in den Keimzellen – hier sind es nur die Hälfte), vollständig dupliziert werden, damit beide entstehenden Tochterzellen wieder den gleichen Chromosomensatz besitzen.
Für diese Duplizierung ist ein hochkomplexer molekularer Apparat verantwortlich, der präzise an der Telomerregion jedes Chromosoms ansetzt. Das Problem ist jedoch, dass bei jeder Zellteilung ein kleines Stück der Telomere nicht mitkopiert werden kann. Dadurch verkürzen sich die Telomere nach jeder Teilung. Irgendwann sind die Telomere so stark verkürzt, dass keine weitere Zellteilung mehr möglich ist.
Wenn eine Zelle sich nicht mehr teilen kann, sollte sie idealerweise den Prozess der natürlichen Apoptose, also des kontrollierten Zelltods (Apoptose), durchlaufen, um Platz für neue, gesunde Zellen zu machen. Mit zunehmendem Alter ist jedoch häufig zu beobachten, dass viele dieser alternden Zellen nicht mehr absterben, sondern stattdessen im Gewebe verbleiben. Diese Zellen nennt man auch „Zombiezellen“ oder seneszente Zellen. Sie erfüllen keine Funktion mehr, stören aber die umliegenden Gewebe, indem sie niederschwellige Entzündungsreaktionen hervorrufen. Auf diese Weise tragen sie zur Gewebealterung bei und fördern die Entstehung von chronischen Krankheiten.
Glücklicherweise verfügt unser Körper über Telomerasen, Enzyme, die in der Lage sind, die Telomerregionen wieder aufzubauen und so die Teilungsfähigkeit der Zellen aufrechtzuerhalten. Leider nimmt auch die Aktivität dieser Telomerasen im Alter ab, was bedeutet, dass der Schutz unserer Chromosomenenden mit der Zeit immer weiter abnimmt und das Altern beschleunigt wird.
BS: Das klingt nach einem komplexen und schwer zu beeinflussenden Prozess. Gibt es dennoch Möglichkeiten, die Telomer-Abnutzung durch unseren Lebensstil zu verlangsamen?
AR: Ja, es gibt einige Ansätze, mit denen wir die Aktivität der Telomerasen fördern und somit die Telomer-Abnutzung verlangsamen können. Ein gesunder Lebensstil mit einem ausgeglichenen Stoffwechsel spielt dabei eine Schlüsselrolle. Studien haben gezeigt, dass regelmäßiger, moderater Sport die Telomerase-Aktivität anregen kann. Bewegung fördert den Stoffwechsel und verbessert die Versorgung der Zellen mit Sauerstoff und Nährstoffen. So können Zellen effizienter arbeiten und besser mit schädlichen Einflüssen umgehen, was die Abnutzung der Telomere verlangsamt.
Und auch hier zeigt das Fasten eine positive Wirkung auf die Telomeraseaktivität. Fastenperioden führen zu einer verbesserten zellulären Autophagie, einem Selbstreinigungsprozess der Zellen, bei dem alte oder geschädigte Zellbestandteile abgebaut und recycelt werden. Dieser Prozess entlastet die Zellen und kann dazu beitragen, dass die Enzyme, die für den Wiederaufbau der Telomerregionen verantwortlich sind, vermehrt aktiv werden. Auf diese Weise unterstützt Fasten die Zellgesundheit und kann die Telomer-Abnutzung zumindest teilweise verlangsamen.
Das Meiden äußerer Einflüsse, ein gesunder Stoffwechsel durch viel Bewegung (Kraft u. Ausdauer) und eine ausgewogene Ernährung reich an Antioxidantien und Mikronährstoffen, ausreichende Nahrungspausen (s. z.B. intermittierendes Fasten) und Schlaf ist wohl der beste Schutz gegen das Altern.
BS: Vielen Dank, Dr. Raab, für diese wertvollen Einblicke. Es ist beruhigend zu wissen, dass wir durch bewusste Entscheidungen Einfluss auf unsere Gesundheit und unser biologisches Alter nehmen können.
Es liegt also in unserer Hand, viele dieser schädlichen Einflüsse zu vermeiden und die Selbstheilungskräfte unseres Körpers zu unterstützen. So können wir dazu beitragen, den Alterungsprozess positiv zu beeinflussen und die genetische Instabilität und die Telomer-Abnutzung – zumindest teilweise – in Schach zu halten.
Für unsere Leser stellen wir noch eine Liste an Lebensmittel und Nährstoffen bereit, zu deren Wirksamkeit in Hinblick auf die Verlangsamung des biologischen Alterungsprozesses wissenschaftliche Nachweise bekannt sind.
Im nächsten Teil unserer Serie beschäftigen wir uns mit dem Thema „Epigenetische Veränderungen“ sowie „Verlust der Proteaseaktivität“ und wie diese unser Altern und unsere Gesundheit beeinflussen.
Bleiben Sie dran!
Teile der Serie
1. Einleitung
2. Genetische Instabilität und Telomerabnutzung
3. Epigenetische Veränderungen und der Verlust der Proteostase
Erschienen in:

Ausgabe Nr. 59 (Nov./Dez. 2024)
Akut geschützt, langfristig gefährdet
Warum unser Gesundheitssystem uns nicht vor chronischen Krankheiten bewahrt
